Kinase Kinetics Array キナーゼアレイ
・目的のキナーゼの基質特異性を網羅的にマッピングできます(図1).
・タイタープレートにして40枚相当の反応が同時に行なえます.
・目的タンパク質の、リン酸化部位のマッピングにご利用いただけます.
・セルライセートや未知タンパク質から、新規キナーゼの探索が行えます(図2).
・リン酸化パターンを比較し、新規バイオマーカーの探索や、シグナルパスウェイの解析などに利用できます.
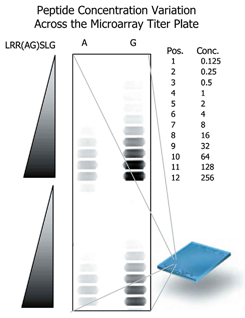
図1.ペプチド配列を異なるモル密度で合成することにより、異なる濃度の基質が得られる.
配列LRRGSLG、LRRASLG(上段:PKA基質配列およびそのアラニン置換配列)、 およびLKRGSLG、LKRASLG(下段:PKC基質配列およびそのアラニン置換配列)を密度(濃度)を変えて合成した.
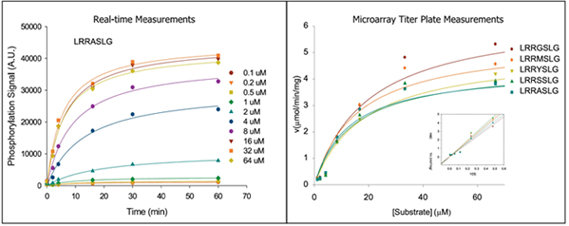
図2.様々な配列および濃度のペプチド基質に対するPKAのリン酸化反応を1アッセイで同時に行った. cAMP-dependent Protein Kinase (PKA); 2,500U 50uL 様々な濃度におけるLRRASLG配列のリン酸化のタイムコース(左図). 様々な配列を持つ基質に対する濃度曲線(右図). Pico-liter titer plate arraysにより数百種のこのようなカーブを同時に測定でき、これらの結果から各ペプチド配列に対するVmaxおよびKmが導きだされる(図3).
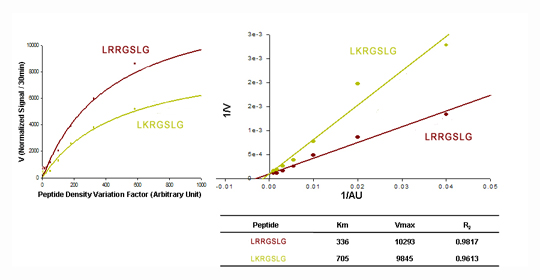
図3.LRRGSLGおよびLKRGSLGのリン酸化反応のMichealis-Menton定数およびKmの決定. 上の結果から線形変換(Lineweaver-Burke analysis)によりLRRGSLGおよびLKRGSLGに対するPKAのVmaxおよびKm値を求めた.

図4.キナーゼ阻害スクリーニングアッセイ.
様々なキナーゼ基質ペプチドに対する阻害定数を1アッセイで同時に測定することにより、キナーゼ阻害の特異性を比較でき、潜在的なリン酸化部位を同定することができます(D1、D2、D3−ペプチド濃度)